| Tips en Trucs artikelen | Hyperlink | Auteur/Copyrights |
|---|---|---|
| Aquariumchemie |
|
Andre de Graaf |
| Een zelf te bouwen goed functionerend oeveraquarium |
|
Loek van der Klugt |
| Flevopoltechnologie |
|
Loek van der Klugt |
door: A. de Graaf
5e druk, april 2009
-
overname van de tekst en
figuren is slechts toegestaan met bronvermelding
AQUARIUM CHEMIE
email :
andre-de-graaf@hetnet.nl
Veel aquarianen bewaren hun meetsets en
PH-ijkbuffers in de kast onder het aquarium. Dit blijkt echter niet
de meest geschikte plaats te zijn. Het is daar veel te warm en de
meeste meetsets en alle ijkbuffers zijn na enkele maanden niet meer
te gebruiken. Veel beter is het om de meetsets en ijkbuffers in de
koelkast te bewaren. Ze blijven dan (met uitzondering van de
ijkbuffer van PH 9) jaren lang goed.
BASISBEGRIPPEN
Moleculen, atomen, elementen
Als we stoffen zoals keukenzout, glas, water, soda
enz. steeds in kleinere stukjes gaan verdelen komen we op een
bepaald moment uit op een punt dat als we verder gaan met opdelen de
eigenschap van het materiaal zou gaan veranderen. De kleinste
stukjes die dan zijn ontstaan worden moleculen genoemd.
Deze moleculen op zich bestaan echter weer uit nog
kleinere deeltjes, de atomen.
Van atomen van dezelfde soort zeggen we dat ze tot
een bepaald element behoren.
In de natuur blijken ruim 90 verschillende elementen
voor te komen. Alle stoffen op aarde bestaan uit een
samenvoeging/verbinding van atomen van één of meerdere van deze
elementen. Daarbij kan een stof opgebouwd zijn uit atomen van één
soort maar ook uit een aantal verschillende elementen.
De verschillende elementen hebben alle een
verschillende één of twee letterige code (het zgn. symbool)
gekregen. Voorbeelden van elementen zijn:
Naam
Code / Symbool
Calcium
Ca
Chloor
Cl
Kalium
K
Koolstof
C
Magnesium
Mg
Natrium
Na
Fosfor
P
Stikstof
N
Waterstof
H
Zuurstof
O
Zwavel
S
Ammoniak
NH3
Diamant
C
Grafiet
C
Koolzuur
CO2
Maagzout / Natriumbicarbonaat
NaHCO3
Nitraat
NO3
Nitriet
NO2
Natriumfosfaat
Na3PO4
Soda / dubbelkoolzure soda
Na2CO3
Water
H2O
Zuurstof
O2
verhoudingen tussen aantallen atomen
Gewichten van atomen
Andere relatieve gewichten van atomen zijn:
Calcium
40,1
Chloor
35,5
Kalium
39,1
Koolstof
12,0
Magnesium
24,3
Natrium
23,0
Stikstof
14,0
Zuurstof
16.0
Zwavel
32,1
IONEN, ZUREN,
LOGEN EN ZOUTEN
Bij de stoffen die uiteenvallen in ionen kan onderscheid gemaakt worden in:
-
zuren :
Bij uiteenvallen komt een H+ deeltje vrij
Zuren die geheel uiteenvallen in een positief en een negatief
ion worden sterke zuren genoemd. Die zuren die slechts gedeeltelijk
uiteenvallen zwakke zuren. Afhankelijk van de mate van uiteenvallen
is het ene zuur sterker dan wel zwakker dan het andere zuur.
.
De positieve ionen worden kationen genoemd en
de negatief geladen ionen anionen.
HARDHEID
a.
TOTAALHARDHEID
(GH)
-
TIJDELIJKE HARDHEID
-
BLIJVENDE HARDHEID
b.
CARBONAATHARDHEID
(KH)
ZUURGRAAD
Bufferende werking
Natuurlijke PH waarden
KOOLZUUR HOEVEELHEID
SAMENHANG PH, KH EN CO2-GEHALTE VAN HET
WATER
|
KH |
PH-waarde |
|||||||||
|
6,2 |
6,4 |
6,6 |
6,8 |
7,0 |
7,2 |
7,4 |
7,6 |
7,8 |
8,0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
25 |
15 |
10 |
6 |
4 |
2 |
1.5 |
1 |
½ |
0 |
|
2 |
50 |
30 |
20 |
13 |
8 |
5 |
3 |
2 |
1 |
½ |
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
75 |
50 |
30 |
20 |
12 |
8 |
5 |
3 |
2 |
1 |
|
4 |
100 |
60 |
40 |
25 |
15 |
10 |
6 |
4 |
2½ |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
125 |
80 |
50 |
32 |
20 |
12 |
8 |
5 |
3 |
2½ |
|
7 |
175 |
110 |
70 |
45 |
28 |
18 |
11 |
7 |
4 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
250 |
160 |
100 |
65 |
40 |
25 |
16 |
10 |
6 |
4 |
|
12 |
300 |
190 |
120 |
75 |
50 |
30 |
19 |
12 |
8 |
5 |
|
|
CO2-gehalte in mg per liter |
|||||||||
KOOLZUURPRODUCTIE /
KOOLZUUROPNAME
6 CO2 + 6 H2O C6H12O6 + 6O2
koolzuur en water worden omgezet in suiker en zuurstof
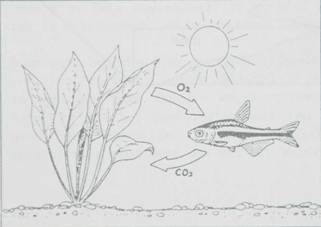
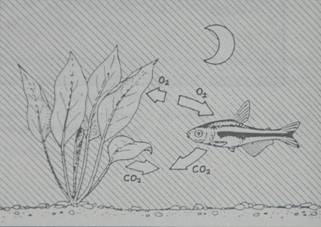 In
onderstaande figuur is te zien dat de planten zuurstof produceren.
Deze wordt door de dieren opgenomen onder afgifte van koolzuur. De
koolzuur wordt door de planten weer opgenomen. Ook planten nemen
zuurstof op en geven koolzuur af. Overdag is de afgifte van zuurstof
en de opname van koolzuur echter veel groter dan 's nachts. De
fotosynthese staat dan stil omdat er geen licht is.
In
onderstaande figuur is te zien dat de planten zuurstof produceren.
Deze wordt door de dieren opgenomen onder afgifte van koolzuur. De
koolzuur wordt door de planten weer opgenomen. Ook planten nemen
zuurstof op en geven koolzuur af. Overdag is de afgifte van zuurstof
en de opname van koolzuur echter veel groter dan 's nachts. De
fotosynthese staat dan stil omdat er geen licht is.
overdag
‘s nachts
Voor een groot gedeelte wordt het koolzuur
geproduceerd door bacteriën en slechts voor een klein gedeelte door
hogere organismen (bv. garnalen, vissen, zoogdieren).
Overdag zal door de opname van koolzuur de PH van
het water stijgen zodat in de avond de PH van het water hoger zal
zijn dan 's morgens vroeg.
Schematische weergave van de koolzuur/zuurstof
kringloop
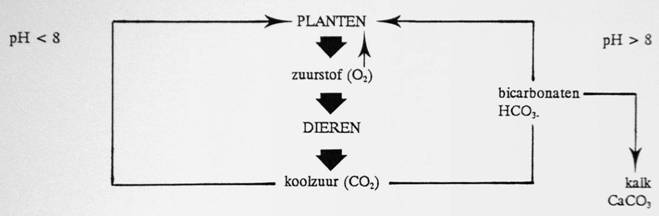 Dit
schema geeft aan dat dieren zuurstof opnemen onder afgifte van
koolzuur. Deze koolzuur wordt door de planten weer opgenomen. Ook
planten nemen zuurstof op. Overdag is de afgifte van zuurstof echter
veel groter dan de opname. ‘nachts neemt de plant alleen zuurstof
op.
Dit
schema geeft aan dat dieren zuurstof opnemen onder afgifte van
koolzuur. Deze koolzuur wordt door de planten weer opgenomen. Ook
planten nemen zuurstof op. Overdag is de afgifte van zuurstof echter
veel groter dan de opname. ‘nachts neemt de plant alleen zuurstof
op.
Biogene Ontkalking
Biogene ontkalking is het proces waarbij door de
planten bicarbonaat (HCO3–) wordt gebruikt
i.p.v. koolzuur. Aangezien de opname van koolzuur ca. 100x
efficiënter gaat dan de opname van bicarbonaat zullen de planten de
voorkeur geven aan koolzuuropname boven bicarbonaatopname.
Bij een PH lager dan 8 is vrij koolzuur aanwezig
(zie fig. blz. 9) en zal dat opgenomen worden. Bij een hogere PH is
er geen vrij koolzuur meer aanwezig maar wel bicarbonaten. Sommige
planten (o.a. hoornblad, Vallisneria, Najas) zijn in staat hieruit
koolzuur vrij te maken. Er ontstaat dan CO32 –
dat zich met het in het water aanwezige Ca2+ verbind tot
kalk. Bij de planten die bicarbonaat opnemen wordt, voornamelijk aan
de onderzijde van het blad, een grijze aanslag aangetroffen. De
bovenzijde is gewoonlijk gewoon groen van kleur.
Het bicarbonaat wordt namelijk opgenomen aan de
bovenzijde van het blad. CO2 wordt daarna in het blad aan
het bicarbonaat onttrokken (zie chemische reactie 1). Aan de
onderzijde van het blad wordt het vrijgekomen OH –
deeltje aan het water afgestaan. Dat deeltje reageert daar met een
ander bicarbonaat-ion (reactie 2) waarbij een carbonaat-ion (CO32
–) wordt gevormd. Dit CO32– reageert met
de aanwezige Ca2+ ionen tot de niet oplosbare stof
Calciumcarbonaat (CaCO3)(reactie 3) die zich afzet op het
blad.
Chemische reacties:
![]() in
blad:
1)
HCO3–
CO2 + OH –
in
blad:
1)
HCO3–
CO2 + OH –
![]() onderzijde
blad:
2)
OH – + HCO32
–
H2O + CO32
–
onderzijde
blad:
2)
OH – + HCO32
–
H2O + CO32
–
![]() 3)
CO32 – + Ca2+
CaCO3
3)
CO32 – + Ca2+
CaCO3
4)
CaCO3 afzetting op onderzijde v.h. blad.
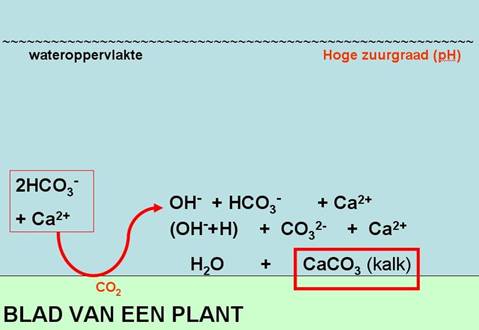
De hoeveelheid koolzuur die d.m.v. biogene
ontkalking wordt opgenomen is veel lager dan bij een lagere
zuurgraad het geval is. De hoeveelheid geproduceerde zuurstof zal
dan ook lager zijn.
ZUURSTOF
De hoeveelheid van een gas die maximaal in water
opgelost kan zijn is afhankelijk van de temperatuur. Hoe hoger de
temperatuur, hoe lager de hoeveelheid opgelost gas. Voor zuurstof
zijn de hoeveelheden als volgt:
|
|
Maximale hoeveelheid
Zuurstof in water |
|
De zwavel- en stikstofverbindingen die zich
bevinden in de afvalstoffen van planten en dieren worden
omgezet in resp. zwavelwaterstof (H2S) (de
bekende lucht van rotte eieren) en ammoniak (NH3).
In aanwezigheid van voldoende zuurstof
worden deze zeer giftige stoffen door de zuurstofbehoevende
(aerobe) bacteriën verder afgebroken tot minder giftige
stoffen. (zie ook blz. 16 en 22).
|
|
|
|
°C |
mg/l |
|
|
|
|
0
1
2
3
4
5
10
15
20
25
30
|
14,54
14,15
13,76
13,41
13,06
12,73
11,27
10,10
9,13
8,34
ca.
7
|
|
|
Indien er veel afvalstoffen in het water zijn zullen
er veel bacteriën nodig zijn om dat af te breken. Er wordt dan veel
zuurstof gebruikt. In stilstaand water zal op die plaatsen, doordat
de transportsnelheid van gassen in stilstaand water erg laag is (ca.
1/100.000 van die in lucht), het zuurstofgehalte dalen en kan een
zuurstof tekort ontstaan. Vervuiling door bv. olieachtige stoffen
die het wateroppervlak afsluiten, kunnen een extra bijdrage aan het
ontstaan van een zuurstof tekort geven doordat er geen zuurstof meer
uit de atmosfeer gehaald kan worden.
Kleine, niet met ander water in verbinding staande
wateren (bv. vijvers) zijn daardoor zeer gevoelig voor vervuiling.
Zorgen voor het weghalen van in het water gevallen bladeren,
voedselresten e.d. is dan ook erg belangrijk. In een zuurstof arm
milieu kunnen ook insecten, kreeftjes en vissen niet meer leven.
Deze sterven af en zorgen voor een nog grotere hoeveelheid
afvalstoffen in het water.
Indien er te weinig zuurstof in het water aanwezig
is kunnen alleen de bacteriën die weinig zuurstof nodig hebben, de
anaërobe bacteriën, zich handhaven en worden ammoniak en
zwavelwaterstof niet verder afgebroken.
Effect van doorluchting / watercirculatie
Water is verzadigd met koolzuur bij ca. 0,5 mg/l.
Het is echter gemakkelijk om een oververzadigde oplossing van
koolzuur te maken.
In het aquarium willen we voor een goede
plantengroei 10-25 mg/l hebben. Bij het doorluchten van het aquarium
zal, vooral in aquaria waar koolzuur wordt toegediend, koolzuur uit
het water worden verwijderd.
De concentratie zuurstof in lucht is ca. 300 mg per liter en in
water ca. 10 mg per liter. Door doorluchting of een andere vorm van
watercirculatie wordt het water in beweging gebracht en wordt
zuurstofarm water naar het wateroppervlak geleid en zuurstofrijk
water naar de bodem. Het zuurstofarme water neemt dan zuurstof op
uit de lucht. Tevens wordt door doorluchting het wateroppervlak
vergroot waardoor de opname van zuurstof versneld wordt. Zuurstof
kan door doorluchting / watercirculatie eenvoudig worden aangevuld.
Te weinig zuurstof in het water blijkt dan ook over het algemeen
geen gevolg te zijn van een gebrekkige productie van zuurstof door
de planten maar van een gebrek aan transport van zuurstof en een
slechte opname van zuurstof vanuit de atmosfeer.
REDOXPOTENTIAAL
Zuurstof is in staat gevaarlijke stoffen in het
water onschadelijk te maken door er zich mee te verbinden. Dit
verbinden met zuurstof noemen we oxydatie. Ook het onttrekken van
waterstof atomen wordt oxydatie genoemd. (De onttrokken waterstof
kan bv. met zuurstof reageren tot H2O.)
Ook andere in het water bevindende stoffen kunnen
een zuurstofatoom afstaan aan een andere verbinding of een
waterstofatoom eruit halen. Ook zijn er verbindingen die het
omgekeerde doen. Deze eigenschap wordt dan reductie genoemd.
Uit de verhouding tussen de hoeveelheden reducerende
en oxiderende stoffen kan de redoxpotentiaal worden berekend.
In stilstaand water zullen op den duur de
reducerende stoffen de oveRhand krijgen.
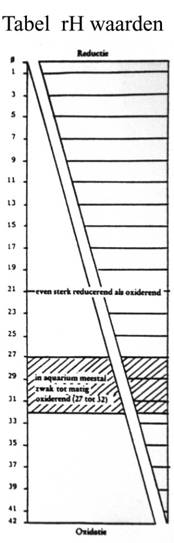
Voor de redoxpotentiaal worden de termen eH en Rh
gebruikt.
De redoxpotentiaal is afhankelijk van de PH zodat
het bij metingen nodig is ook de PH nauwkeurig te meten. Een zeer
hoge Rh duidt op zeer zuiver, zuurstofrijk water (bergbeek,
koraalzee).
 Oxydatie
verbinden met zuurstof of
Oxydatie
verbinden met zuurstof of
onttrekken van waterstof
Reductie
onttrekken van zuurstof of
verbinden met waterstof
Redoxpotentiaal
verhouding tussen oxiderende
en reducerende stoffen
INVLOED OP AFBRAAKPROCESSEN
De H2S omzetting tot sulfaat en de
ammoniak omzetting tot nitraat vinden alleen plaats als er meer
oxiderende dan reducerende stoffen in het water zijn.
M.a.w. als een hoge redoxpotentiaal aanwezig is.
Blauwe alg kan het gevolg zijn van het stagneren van
afbraakprocessen.
NATUURLIJKE WAARDEN
Eh zuurstofloos water
-0,1 V
Eh zuurstofrijk water
+0,5 V
Eh bodemgrond
vaak < -0,1 V
De Rh kan uit de Eh berekend worden met de formule:
Rh = 10087 . Eh/T + 2 PH
(T in Kelvin)
ZWAVELWATERSTOF
(H2S)
Vissen en planten zorgen in het water voor de
productie van afvalstoffen.
Deze worden door bacteriën afgebroken tot het
gevaarlijke zwavelwaterstof (H2S).
Onder invloed van weer andere bacteriën kan bij een
gunstige redoxpotentiaal (een voldoende hoeveelheid zuurstof) het
giftige zwavelwaterstof omgezet worden in sulfaat. (SO42
–).
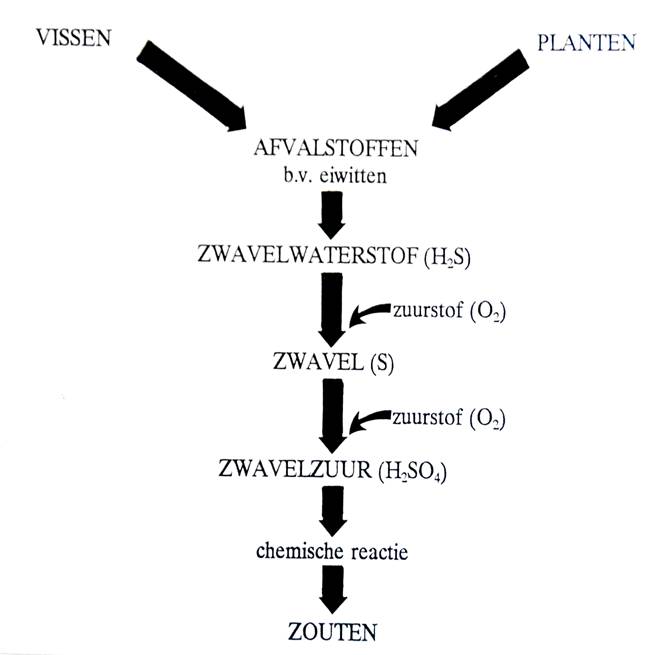 In
een dichtgeslibde bodem zal de zuurstofhoeveelheid dalen. De
redoxpotentiaal daalt en de gevormde zwavelwaterstof zal niet worden
omgezet.
In
een dichtgeslibde bodem zal de zuurstofhoeveelheid dalen. De
redoxpotentiaal daalt en de gevormde zwavelwaterstof zal niet worden
omgezet.
OSMOSE
Osmose is het verplaatsen van water door bv. de wand
van een cel (of membraan) ten gevolge van een verschil in
hoeveelheid opgeloste stoffen per liter water. (Ofwel een verschil
in concentratie aan opgeloste stoffen). De wanden van cellen laten
daarbij alleen water door en niet de opgeloste stoffen. Het water
gaat daarbij van de kant waar de concentratie laag is naar de kant
waar de concentratie hoog is.
Door die verplaatsing van water wordt het verschil
in concentratie kleiner. De druk op de celwand, van binnen uit
gezien, zal verminderen als er water uitgaat en vermeerderen als er
water binnenkomt.
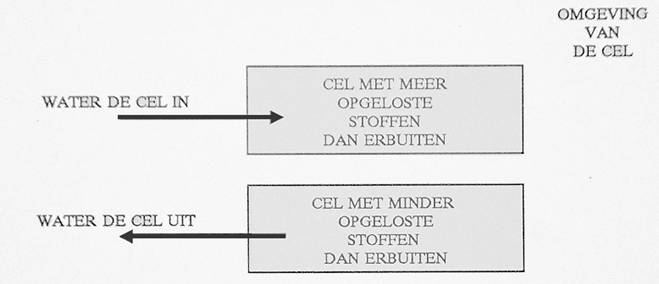
Het
gevolg is dat de cel kleiner resp. groter wordt om dit drukverschil
op te vangen. Het drukverschil (de osmotische druk) is afhankelijk
van het verschil in zoutconcentratie tussen de beide zijden van de
membraan.

Bij eieren van vissen is osmose een belangrijke
factor bij het al dan niet uitkomen van de eieren.
Als de concentratie aan opgeloste stoffen in het
water buiten het ei lager is dan in het ei gaat het water het ei in
(a). De druk op de binnenzijde van het ei-omhulsel wordt groter en
de jonge vis kan makkelijker het omhulsel doorbreken.
Als de concentratie aan opgeloste stoffen buiten het
ei hoger is wordt het water uit het ei getrokken en wordt de druk op
de binnenzijde van het ei-omhulsel lager. Het ei wordt daardoor
kleiner (b). De jonge vis heeft dan meer moeite om uit het ei te
komen. Het kan er zelfs toe leiden dat eieren niet uit kunnen komen.
In tegenstelling tot de eieren kunnen de meeste
vissen kunnen zich redelijk goed aanpassen aan andere osmotische
waarden dan waar zij in de natuur leven.
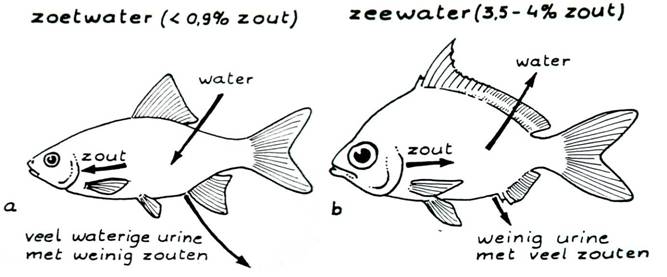
Zowel zoet- als zeewatervissen blijken ca. 0,9% zout
te bevatten. Zoetwatervissen bezitten daardoor een hoger zoutgehalte
in het lichaam dan daarbuiten. Er zal daarom water door de huid van
de vis naar binnen gaan. Omdat daardoor de zoutconcentratie in de
vis daalt wordt via de kieuwen extra zout uit het water opgenomen.
Tevens wordt er veel waterige urine met weinig zout uitgescheiden
(zie tekening a). Bij zeewatervissen daarentegen zal doordat ze
minder zout bevatten dan hun omgeving water aan het lichaam worden
onttrokken. Via de kieuwen wordt daartoe zout uitgescheiden. Tevens
wordt weinig urine maar met veel zouten uitgescheiden. (zie tekening
b)
OMGEKEERDE OSMOSE
Bij osmose ging water van een milieu met een lage
concentratie aan opgeloste stoffen naar een milieu met hoge
concentratie. De verplaatsing van water veroorzaakt een drukverschil
tussen de beide milieus. Het maximale drukverschil is afhankelijk
van het verschil in zoutconcentratie. Hoe groter het verschil in de
hoeveelheid opgeloste stoffen, hoe hoger het maximale drukverschil.
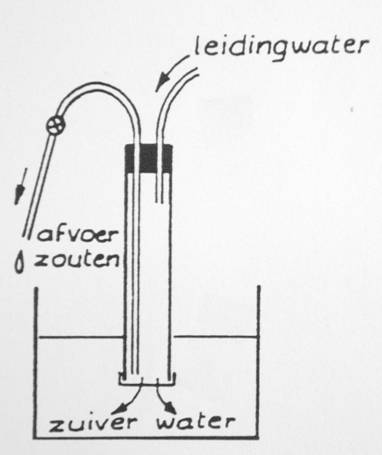
Bij omgekeerde osmose, bv. om water te zuiveren,
wordt dit principe gebruikt om water te zuiveren. Hier wordt gezorgd
voor een drukverschil tussen de beide zijden van het
(osmose)membraan door het te zuiveren water onder druk tegen het
membraan te persen. In het begin is aan beide zijden van het
membraan de hoeveelheid opgeloste stoffen gelijk. Door het
drukverschil tussen de beide zijden van het membraan wordt water
door het membraan geperst.
Doordat alleen water door de membraan heen kan
blijven de opgeloste stoffen achter en kan aan de andere zijde van
het membraan het "gedemineraliseerde" water, dat vaak osmosewater
wordt genoemd, worden opgevangen.
Aangezien het water aan de zijde van het membraan
waar het tegenaan wordt geperst een steeds hogere concentratie aan
opgeloste stoffen zal gaan bevatten zal door de "gewone" osmose het
doorlaten van water gaan afnemen. Om het zuiveren van water door te
laten gaan wordt gebruikt water afgevoerd en nieuw te zuiveren water
toegevoerd.
IONENWISSELAARS
Ionenwisselaars zijn stoffen die bepaalde elektrisch
geladen deeltjes (ionen) uit het water halen en er andere ionen voor
terug geeft. De ionen die worden teruggegeven zijn tevoren aan de
ionenwisselaar gebonden.
M.a.w. er zit een deeltje A aan de wisselaar vast en
er komt een deeltje B langs dat beter met de wisselaar bindt dan
deeltje A, dan laat deeltje A los en deeltje B blijft aan de
wisselaar vastzitten.
Een ionenwisselaar die alle ionen (zouten) uit het
water haalt en er water voor terug geeft wordt tevoren "geladen"
door een deel van de wisselaar te spoelen met natriumhydroxide (NaOH)
of soda (Na2CO3) en het andere deel met
zoutzuur.
Als er met soda wordt gewerkt ontstaat er
koolzuurrijk water dat voor gebruik goed doorgelucht moet worden
aangezien het koolzuurgehalte dodelijk is voor de vissen.
Het "laden" van een ionenwisselaar is eigenlijk geen
werk voor een amateur. Zoutzuur en natriumhydroxide zijn nogal
gevaarlijke stoffen.
Een veel meer gebruikte ionenwisselaar is het zgn.
onthardingsapparaat. Deze ionenwisselaar haalt alleen de stoffen die
het water "hard" maken uit het water en geeft daar over het algemeen
NaCl (keukenzout) voor terug. Dit type ionenwisselaar wordt namelijk
meestal met keukenzout geladen (geregenereerd).
Het water dat uit een onthardingsapparaat komt is
wel geschikt voor het houden van vissen die water met een lage
hardheid verlangen, maar niet voor vissen die daarnaast ook een laag
totaal zoutgehalte verlangen zoals bv. de discusvis.
AMMONIAK
Bij de afbraak van planten- en voedselresten en de
afbraak van voedingsstoffen in dieren wordt ammonium NH4+gevormd.
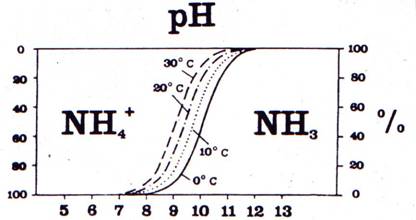
Afhankelijk van de zuurgraad (PH) en temperatuur van het water wordt
dit voor een deel omgezet in ammoniak (NH3) (zie figuur
en tabel) dat ca. 100x giftiger is dan ammonium.
![]() NH4+
+ OH –
NH3 + H2O
NH4+
+ OH –
NH3 + H2O
 Een
ammoniakconcentratie van 0,2 - 1,0 mg/l zorgt bij vissen voor een
versnelde ademhaling en 1,0 - 2,5 mg/l ammoniak is vaak dodelijk.
Een
ammoniakconcentratie van 0,2 - 1,0 mg/l zorgt bij vissen voor een
versnelde ademhaling en 1,0 - 2,5 mg/l ammoniak is vaak dodelijk.
Bij 20°C:
|
PH |
% NH3 |
% NH4+ |
|
|
6,0
6,5
7,0
7,5
8,0
8,5 |
0,06
0,18
0,6
1,8
5,4
15,3 |
99,94
99,82
99,4
98,2
94,6
84,7 |
Bij een PH onder de 7 blijkt nagenoeg geen ammoniak
aanwezig te zijn. Bij een PH van 8 en een temperatuur van
Ammoniakvergiftiging door PH verhoging.
Bij verhoging van de PH (bv. bij aquaria voor
Malawi- en Tanganjikacichliden) is het belangrijk om eerst de
ammoniumconcentratie te meten en uit te rekenen m.b.v.. bovenstaande
tabel hoeveel ammoniak dat bij de gewenste PH zou betekenen. Het is
zeer goed denkbaar dat bij PH 7 geen gevaar aanwezig is maar dat bij
PH 8,5 een veel te hoge ammoniakconcentratie ontstaat.
Bijvoorbeeld:
Bij 10 mg ammonium per liter en een PH van 7 is 0,06
mg (0,6% van 10 mg/l) ammoniak per liter aanwezig en zijn er geen
problemen. Als de PH daarna naar 8,5 wordt verhoogd gaat de
ammoniakconcentratie naar 1,5 mg per liter (15,3% van 10mg/l). Dat
kan de dood van de vissen betekenen.
STIKSTOFCYCLUS
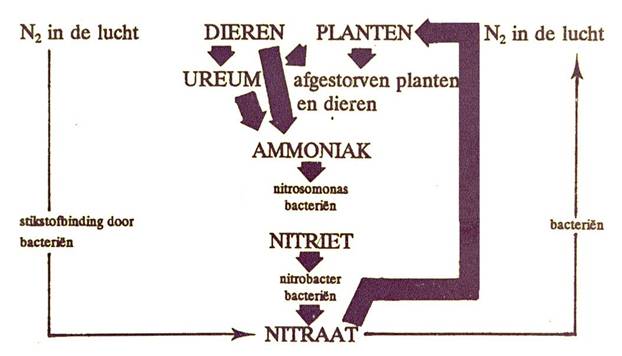
Afbraak van ammoniak
NB: In bovenstaande figuur staat ureum als
afvalproduct van dieren. Vissen produceren echter geen ureumhoudende
urine (zoals zoogdieren) maar ammoniakhoudende urine zodat de
afbraak van ureum naar ammoniak daar niet noodzakelijk is..
Ammoniak wordt door de nitrosomas-bacteriën
afgebroken tot nitriet (NO2–)
![]() NH3
+ 3O2
2NO2– + 2H+ + H2O
NH3
+ 3O2
2NO2– + 2H+ + H2O
waarna de nitrobacter-bacteriën het nitriet afbreken
tot nitraat (NO3-).
![]() 2NO2–
+ O2
2NO3–
2NO2–
+ O2
2NO3–
De afbraak van ammoniak tot nitraat wordt
nitrificatie genoemd. Zoals uit bovenstaande chemische formules
blijkt zijn voor elk ammoniakdeeltje 4 zuurstofdeeltjes nodig om het
om te zetten tot nitraat. De minimale zuurstofconcentratie om het
proces te laten verlopen blijkt 0,5 mg/l te zijn. Bij een goede
doorstroming in het aquarium zal dit, gezien het feit dat de
maximale zuurstof verzadiging, afhankelijk van de temperatuur, 7 tot
10 mg/l bedraagt geen probleem opleveren. Op plaatsen waar weinig
waterbeweging is, zgn."dooie" hoeken in het aquarium of in een
dichtgeslibde bodem, kan de zuurstofconcentratie wel te laag worden.
Ook de PH blijkt van invloed te zijn op de afbraak van ammoniak.
Beneden PH 6,5 en boven PH 8,5 daalt de afbraaksnelheid zeer sterk.
Als de afbraak niet goed verloopt kan er een te hoge concentratie
aan ammoniak resp. nitriet ontstaan. Het nitrietgehalte dient
maximaal 0,15 mg per liter te bedragen.
Het ontstane nitraat dient weer als voedingsstof
voor de planten. Een kleine hoeveelheid nitraat wordt door bacteriën
omgezet in stikstof (N2) dat aan de lucht wordt afgestaan
of rechtstreeks uit stikstof gevormd.
Een slechte afbraak kan ontstaan in water waarin
(plaatselijk) te weinig zuurstof aanwezig is (de redoxpotentiaal is
laag). Ook is het mogelijk dat er denitrificatie optreedt. Het
relatief onschadelijke nitraat wordt dan omgezet in het veel
gevaarlijker nitriet. Nitraat is het eindproduct van de afbraak. Het
wordt door de planten opgenomen als voedingsstof. 10 - 30 mg nitraat
per liter is voor de planten voldoende. Een te hoog nitraatgehalte
(meer dan 150 mg per liter) remt de plantengroei en schaadt de
gezondheid van de vissen. Bij 80 tot 100 mg nitraat per liter water
stagneert de plantengroei. Het resultaat is dan een ophoping van
afvalstoffen hetgeen een voedingsbodem kan betekenen voor (vooral
blauwe) algen.
De blauwe algen (eigenlijk cyanobacteriën) kunnen
aangezien ze minder zuurstof nodig hebben groeien.
IJZER
IJzer is een sporenelement in het aquarium. Het
zorgt o.a. voor de rode kleur in de planten. Bij gebrek ontstaat
ijzerchlorose (te zien als geel worden van o.a. Hygrophilasoorten).
Planten kunnen ijzer alleen opnemen in de Fe2+vorm.
Aangezien Fe2+ in een zuurstofrijk milieu
omgezet (geoxideerd) wordt in Fe3+ is het toevoegen van
ijzerchloride (FeCl2) om de ijzerconcentratie te veRhogen
niet nuttig.
Een beter resultaat wordt bereikt met aan zgn.
chelatoren gebonden ijzer, zoals Fe2+-EDTA (natrium ferri
ethyleendiaminotetra-acetaat). In de tuinbouw wordt deze stof
aangeboden onder de naam Fetrilon. Deze stof is goed oplosbaar in
water en planten kunnen het ijzer uit deze stof vrijmaken. Fe2+-EDTA
is echter het meest stabiel bij een PH van 8 en hoger en niet bij
een PH van 6,5-7 zodat een regelmatige toevoeging noodzakelijk is.
Er zijn inmiddels chelatoren ontwikkeld die
stabieler zijn bij PH 7. Eén van deze stoffen is Fe2+-EDDHA
(natrium ferri ethyleendiamine bis(2-hydroxyPHenylacetaat)). In de
tuinbouw is deze stof o.a. bekend onder de naam LibFer SP. Diverse
aquariumliefhebbers hebben al met succes van een de nieuwe
chelatoren gebruik gemaakt.
Fe3+ en ionen van zware metalen zoals
kwik (Hg), lood (Pb), koper (Cu) binden zich beter aan EDTA en EDDHA
dan Fe2+ zodat, als deze ionen aanwezig zijn in het
aquarium het Fe2+ wordt losgemaakt van de chelator en
indien het niet snel wordt opgenomen wordt geoxideerd.
Een ijzerconcentratie van 0,1 mg/l is voldoende voor
de aquariumplanten. Aangezien slechts ca. 5% van de Fe-EDTA of
Fe-EDDHA verbinding afkomstig is van ijzer dient ca. 2 mg/l van de
Fe-EDTA of Fe-EDDHA te worden toegevoegd.
IJzer rechtstreeks in de bodem brengen is ook
mogelijk. Dit kan bv. in de vorm van ijzerhoudende klei. Het "oude"
middel: "roestige spijkers in de bodem" is niet zo vreemd aangezien
de bodem meestal zuurstof arm is. Het ijzer wordt dan niet
geoxideerd tot de Fe3+ vorm maar blijft in de Fe2+
vorm of wordt zelfs gereduceerd tot de Fe2+ vorm.
GELEIDBAARHEID
Bij het houden van de meeste aquariumvissen en
-planten is het meten van de geleidbaarheid van het water niet
noodzakelijk. Indien echter goede kweekresultaten gewenst zijn dient
wel rekening met de geleidbaarheid gehouden te worden.
De geleidbaarheid is een maat voor de hoeveelheid
opgeloste zouten. Zouten zijn stoffen die een belangrijke invloed
hebben op de osmotische processen in het aquarium
(zie blz. 5). Hoe meer zout, des te hoger is de
geleidbaarheid. De geleidbaarheid wordt uitgedrukt in μS (micro
Siemens). Een hogere geleidbaarheid wil ook zeggen een lagere
elektrische weerstand. Geleidbaarheid en weerstand zijn aan elkaar
gerelateerd: 1 Ω (Ohm)
= 1 / S (Siemens)
Ter informatie:
-
550 mg zuiver keukenzout per liter gedestilleerd water geeft
een geleidbaarheid van 1000 μS.
-
zuiver water met een PH van 5
ca.
4
μS
-
zuiver water met een PH van 4
ca. 40
μS
-
zuiver water met een PH van 3
ca. 400
μS
-
1°DH
ca. 50
μS
-
gezelschapsaquarium
200-1000 μS
-
brakwater
ca. 14000 μS
-
Waddenzee
ca. 25000 μS
-
Noordzee
ca. 40000 μS
FOSFAAT
Fosfaat is één van de veroorzakers van algenbloei.
Door toevoeging van ijzerchloride (FeCl2) aan het water
gaat het ijzer een verbinding aan met het fosfaat en vormt een niet
oplosbare verbinding die op de bodem terecht komt. Voor het wegnemen
van fosfaat wordt 10 mg ijzerchloride per liter water geadviseerd.
Na een week kan indien nodig een zelfde hoeveelheid worden gegeven.
In een aquarium dient de concentratie fosfaat niet
boven de 0,1 mg/l te komen.
|
WATERSAMENSTELLING |
|
|
|
PH
KH
GH
NO2–
NO3–
μS |
|
|
°DH
°DH
mg/l
mg/l
(max.)
(max.) |
|
Gezelschapsaquarium
Discusvissen
Malawimeer
Tanganjikameer
Zuiver water |
6½-7½
3-15
3-20
0,1
80
200-900
6-7
0,1-3
0,1-5
0,05
40
10-200
7,8-8½
7
4½
0,1
80
210-235
8½-9
17
9
0,05
40
600
7
0
0
0
0
0,05 |
|
WIJZIGEN VAN DE WATERSAMENSTELLING |
||
|
|
verhogen door bv. |
verlagen door bv. |
|
μS |
toevoegen van zout
NaCl geen hardheid verhoging
CaCl2 tevens GH verhoging
NaHCO3 tevens KH verhoging |
ionenwisselaar |
|
PH |
natriumbicarbonaat (NaHCO3)
soda (Na2CO3) |
turfextract (humuszuren)
koolzuur (CO2) |
|
KH |
Natriumbicarbonaat
soda |
ionenwisselaar |
|
GH |
magnesiumchloride (MgCl2)
calciumchloride (CaCl2) |
Ionenwisselaar |
|
Fe2+ |
ijzer-EDTA (bv. fetrilon) |
n.v.t. |
|
NO3–
NO2–
NH3
NH4+ |
|
waterverversing + enten met water uit een
aquarium met goede bacteriën werking |
|
PO42- |
Kaliumfosfaat |
waterverversen |
REDFIELD RATIO
Enkele jaren geleden werd het belang van de
verhouding “Stikstof / Fosfaat (N/P)” voor het aquarium ontdekt.
Begin 2004 werd dit in het blad “Het Aquarium” uitvoerig door C.
Buddendorf beschreven.
A.C. Redfield ontdekte al in 1934 dat in alle
oceanen een vast verhouding tussen stikstof en fosfaat in het water
aanwezig was maar het belang voor aquariumhouders werd tot voor kort
nog niet gezien.
Het blijkt dat in blauwe algen meestal voorkomen in
water met een N/P ratio van 5:1 en groene algen bij een ratio 30:1.
Planten blijken het goed te doen bij een ratio van 16:1
Onderstaande tabel maakt het mogelijk zonder
rekenwerk de Redfieldratio te bepalen.
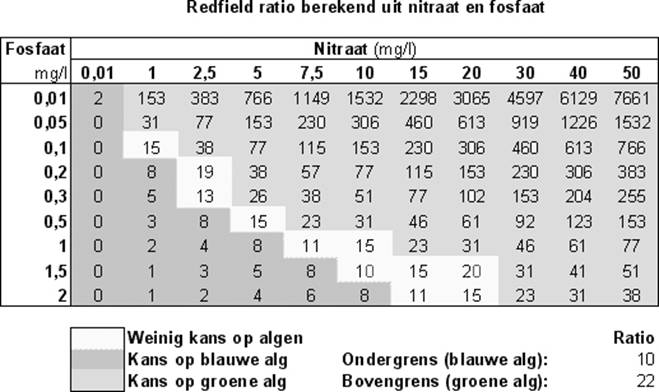
Corrigeren van de Redfieldratio
Bij een Redfieldratio groter dan 16
Kaliumfosfaat (K2HPO4) toedienen
Bij een Redfieldratio kleiner dan 16
Kaliumnitraat (KNO3) toedienen
Voor het berekenen van de hoeveelheid Kaliumfosfaat
en/of Kaliumnitraat is een “rekenmachine” ontwikkeld. Deze kunt u
vinden op de internetsite:
http://www.xs4all.nl/~buddendo/aquarium/redfield.htm
Bij grote hoeveelheden nitraat en/of fosfaat wordt
daarbij tevens waterverversen aangeraden omdat anders erg veel van
één van beide stoffen moet worden toegediend.
NB: genoemde chemicaliën zijn niet of zeer moeilijk
te verkrijgen. Neem indien nodig contact met mij op om de stoffen te
verkrijgen.
ENKELE TOEVOEGINGEN VOOR "DESKUNDIGE"
-
Ik realiseer mij dat de teksten chemisch gezien niet overal
juist zijn. Zo wordt er overal H+ geschreven i.p.v. H3O+.
Deze 'tekortkoming' maakt de tekst voor de meeste aquarianen beter
leesbaar is.
In de berekeningen m.b.t. de koolzuurconcentratie (blz.9) uit
de PH en de KH wordt de H2CO3-concentratie
berekend. Het H2CO3 is in water in evenwicht
met het opgeloste CO2 in water waarbij het evenwicht
sterk aan de CO2 kant ligt. Als alle H2CO3
direct afgebroken wordt, dan is er geen H2CO3
aanwezig en gaat het
evenwicht H2CO3 → HCO3–
+ H+ (pKa = 6,46) naar links aflopen. De KH
daalt dan naar 0. Dit is niet zo omdat de reactiesnelheid waarmee
het H2CO3 wordt omgezet in CO2 zeer
laag is zodat gevormde H2CO3 nog geruime tijd
zal blijven bestaan.
In de tabel, waarvan de getallen afkomstig zijn van Velda, is
de concentratie CO2 opgegeven die ontstaat als alle H2CO3
wordt omgezet in CO2, dus niet de reële CO2
concentratie.
In diverse KH/PH-tabellen worden andere CO2-concentraties
genoemd. Zover ik heb kunnen nagaan is dit een gevolg van
verschillen in de PKa-waarde die gebruikt is. Velda
gebruikt 6,4 , Kasselbeer in "Aquarium Heute" een waarde van 6,25 en
in "Quantitative Inorganic Analysis", A.I. Vogel wordt een waarde
van 6,37 aangegeven.
Herkomst tekeningen:
blz. 10, 17, 18
en 19:
Erik Schoubs: Water voor het zoetwateraquarium 1990
blz. 26:
C. Buddendorf:
http://www.xs4all.nl/~buddendo/aquarium/redfield.htm
Eventueel kan een kabelverwarming of iets dergelijks voor een droog of extra warm plekje zorgen.
Aandachtspunten
- gewenst type biotoop: tropisch of subtropisch, vochtig of nevelwoud, beekdoorsnede met oever of meer moerassig;
Materialen
Afmetingen
Inzichtelijkheid
Veiligheid
Vervorming
Decoratiematerialen
Draagconstructie
Ombouw
Lichteiland
Watervoorraadvat
Wateropvanggoot met overloop- / droogloopbeveiliging
SYSTEMEN VOOR HET BEKLEDEN VAN WANDEN EN HET MAKEN VAN KUNSTMATIGE ROTSEN, KEIEN, STRONKEN EN TAKKEN
Inleiding
Flevopoltechnologie: Een systeem voor het maken van kunsttakken en -stronken en het bekleden van wanden en oevers
Laatste ontwikkelingen: Consequentie van het goed groeien van epifyten en mossen op ondergronden van Flevopol en potgrond is dat die plantjes de potgrond ‘opeten’. Dat is mede een belangrijke reden dat het systeem toch minder duurzaam kan blijken te zijn dan gehoopt. Met deze ervaring/dit inzicht in gedachten zijn leden van Studievereniging Het Paludarium ertoe overgegaan Flevopol Uni onverdund te gebruiken en in plaats van potgrond nog alleen poederklei (fijngestampte gedroogde klei uit de tuin bijvoorbeeld) met wat fijn zand toe te passen. De werkwijze is nu: poederklei vermengen met wat fijn zand en dan pure Flevopol toevoegen tot een smeerbare substantie ontstaat. Die wordt dan met de hand (gebruik beslist huishoudhandschoenen!) of met een slap plamuurmes op de ondergrond aangebracht. Als een donkerder kleur gewenst is, dan mengt men door de droge bestanddelen nog wat fijn gemalen (elektrische koffiemolen!) houtskool. Met houtskoolpoeder door de (pure) Flevopol maak je een soort verf. Daarin kun je ook het te omwikkelen framemateriaal drenken. Dan ben je in één keer klaar! Ronald de Mol doet voor ‘groot werk’ ook poeder-tegellijm door het mengsel en voegt ook verschillende kleurstoffen toe om wat variatie in de kleur te krijgen.
Tegellijmtechnologie: Geschikt voor oersterk wandbekledingssysteem voor aqua-vivaria
Hybridesysteem
In hobbyzaken wordt Paverpol, Pretex en/of Powertex verkocht. Dat wordt gebruikt voor het maken van tuinbeelden. Zie www.paverpol.com. Je drenkt er (repen) lappen in van een stof die het materiaal goed in de vezels opneemt (aanbevolen wordt gebruik te maken van oude T-shirts) en wikkelt die om een draagcontructie. Na droging die overigens heel veel sneller verloopt dan bij Flevopol, is het materiaal watervast. Paverpol wordt thans (augustus/september 2006) in een nieuw gebouwd paludarium toegepast. De vraag is hoe het zich houdt bij voortdurend nat zijn. Het materiaal wordt transparant, maar ook in diverse kleuren geleverd. De transparante vorm kun je met behulp van kleurpoeders op de gewenste kleur brengen. Let op: die kleur is na droging geheel anders dan in de pot, want het spul is in de pot wit. Transparant is het past na droging. Daarom moet je ook tamelijk veel kleurstof toevoegen om een dekkende kleur te krijgen. Gebleken is al dat de kleur van het doek invloed heeft op de kleur na uitharden. Het gebruik van donker doek kan een voordeel zijn. Met acrylverf op waterbasis kun je achteraf nog bijkleuren.

Interieur in opbouw. Bomen en wortels zijn uitgevoerd in geplastificeerd dubbeltjesgaas. Het gaas is omwonden met zelfklevend stukadoorsgaas. Dat is vervolgens aangestreken met een papje van cement-tegellijm, aangemaakt met Flevopol Uni en water. Na droging van die primer- en ‘dichtsmeer’laag is het Flevopol-potgrondmengsel aangebracht. Daarbij bewees een slap plamuurmes goede diensten. Rubber huishoudhandschoenen bleken onontbeerlijk: het mengsel is na opdrogen haast niet van de handen te verwijderen!Langs de stam van de centrale en afgeknotte boom vloeit continu water dat opborrelt uit het hart van de stam. Die stam begroeide prachtig met Java- en levermos en ook Javavaren deed het er goed op. Langs de wanden vloeide drie maal daags gedurende 5 minuten water. Helaas, na een jaar traden al de eerste teken van verval op …
Let wel: bij deze toepassing werd Flevopol nog met 3 delen water verdund en er werd met vochtige potgrond gewerkt.
 |
Bezoek deze website als u een winkel bezoekt waar de dieren niet optimaal worden verzorgd. Hier kunt u er melding van maken, ook is er te zien welke dierenwinkels al zijn bezocht! |
